穀物中含有多種金屬離子,大部分對於身體健康有重要作用,其含量範圍集中在10-100 µg/g,屬於微量分析。對於金屬的處理,大部分的現有文(wén)獻采取的是以混合強酸加熱並溶解的方法,但是這種方法本身極具危險(xiǎn)性,而且環境有極大的影響。所以本次實驗(yàn)中選擇進行長(zhǎng)時間的灰化(huà)以除去(qù)有機物,代替酸解的方法。
對於金屬的微量分析,分光光度法靈敏度高(gāo),易於操作(zuò),是當前十分經(jīng)典的測量微量金屬的方法。但分光光度法存在著準確(què)度極差的缺點,所以我們希望找到可以(yǐ)全部替(tì)代或部分替代分光光度的方法。滴定法時(shí)常用的準(zhǔn)確分析的方法,誤差(chà)極小,EDTA是一種極強(qiáng)的絡合劑,可以和多種金屬離子絡合(hé),常(cháng)用來測量金屬離子的含量。因此,本實驗將(jiāng)這兩種方法結合(hé),采用
實驗電熱(rè)板消解加(jiā)熱測量穀物中的金屬含量。

實(shí)驗過程
儀器與試劑
實驗電熱板(bǎn)HT-200(格丹納)
紫外(wài)可見分光光度計
基準碳酸鈣,鐵標準溶液,基準氧(yǎng)化鋅,六水合氯(lǜ)化鎂,1%鈣指示劑,鋅試劑固體,0.20%鄰二氨菲溶液,pH-8.8的硼砂硼酸緩衝溶液
實驗方法
1.樣品處理
稱取20.0g樣品於坩堝中,先在實驗電熱板(bǎn)上預加熱蒸發至無水(shuǐ)分(fèn),固體呈黑色(sè),轉(zhuǎn)移至馬弗爐,加入適量濃硝酸,灼(zhuó)燒至固體呈灰白色。用5%硝(xiāo)酸(suān)溶解殘(cán)留固體並定容至100mL。
2.標準溶液配製。
3.鈣鎂(měi)含量測定(dìng)
1)鈣鎂總量測(cè)定
利用EDTA與鈣(gài)鎂絡合的反應,在溶(róng)液中加入三乙(yǐ)醇胺掩蔽鐵離子的幹擾(rǎo),再加入適量氨性緩衝溶液,以EBT為指示劑滴定溶液中的鈣鎂總量。
2)鈣含量(liàng)測定
在溶液中(zhōng)加入氫氧化鈉溶液調節pH 至11-12,以鈣指示劑(jì)為指示劑,用EDTA標準溶液滴(dī)定鈣離子含量。
4.鋅含量測定
在溶液中加入三乙醇胺掩蔽鐵離子,加入4mL鋅試劑,再(zài)加入(rù) 3mL硼砂硼(péng)酸緩衝溶(róng)液調節(jiē)pH 至8.8,用蒸餾水(shuǐ)稀釋至25.0mL,用分光(guāng)光度計在618nm 處測定吸光度。
5.鐵含量測定
在溶液中加入1.0mL鹽酸羥胺,混勻靜(jìng)置2min後加入1.0mL鄰二氮菲溶液和2.0mL乙酸(suān)鈉,加水稀釋至25.0mL,在510nm測(cè)定吸光度。
結果與討(tǎo)論

實際樣品中離子濃度(dù)的測定(dìng)
樣品(pǐn)經過長時間灰化後仍有少量(liàng)紫色物質存在,可能是其他離子或殘餘有機物。灰化後(hòu),大米樣(yàng)品殘(cán)餘量極低,可能是誤差(chà)增大的原(yuán)因之一。
最終ICP測試數據顯示:
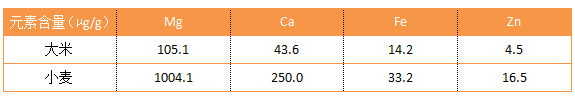
與所測得(dé)的數據相(xiàng)差較大,推測原因是對於實際樣品中的離子環境估計不足,仍存在很多未知離子的幹擾,需要進一步的研究。
總結(jié)
實驗最終探索出了(le)一條基本可以確定穀(gǔ)物重金屬含量(liàng)的方案,但誤差(chà)較大,仍存在(zài)許多地方可以改進。由於時間原因,並未進行更深入的探索及研究。最終的樣品體係中存在許多雜離子,所采取的實驗方(fāng)案並不能全部(bù)消除影響。本次實驗中的格丹納實(shí)驗電熱板(bǎn)HT-200采用了(le)陶(táo)瓷板加熱體(tǐ)發熱提供高(gāo)溫熱量讓樣品(pǐn)加熱,使樣品受熱麵積(jī)更加的均勻。並且是分體控製方式,在通風櫥外進行(háng)控製加熱,科研人(rén)員可以遠離酸(suān)霧和熱量,安全又方(fāng)便。
 020-87026501
020-87026501






 全國服務熱線
全國服務熱線 掃一掃 微信二維碼
掃一掃 微信二維碼